Post n. 32
L’universo ha
avuto origine 13,6 miliardi di anni fa. Fu proprio il Big Bang, l’origine
dell’universo, a porre le premesse per l’origine della vita, perché fu da
quell’origine che si formarono gli elementi chimici.
Nei post già pubblicati abbiamo descritto
l’origine degli elementi e l’origine, dalla materia inanimata, di sostanze
fondamentali per l’origine della vita in particolare amminoacidi, formaldeide
(HCHO) e acido cianidrico(HCN). Inoltre si è anche descritto ampiamente come
l’argilla, secondo l’ipotesi di Bernal, abbia potuto selezionare, accumulare e
proteggere queste sostanze fondamentali. Le argille hanno funzionato quindi da
agente fisico regolatore e un ruolo fondamentale deve aver avuto la silice
colloidale. Questa ipotesi spiega con un modello unico selezione, accumulo e
formazione dei polipeptidi, e ci indica anche simultaneità e localizzazione.
Infatti, non è di nessun interesse che uno di questi processi avvenga al polo
nord, un altro all’equatore e l’altro al polo sud ed in condizioni
chimico-fisiche completamente diverse. E ancora, non è di nessun interesse se
ad un dato istante vengono selezionati gli amminoacidi, da questi dopo un mese
vengono selezionati i levo e dopo un anno si ha la catalisi
Si pone allora la domanda: come è avvenuta la
sintesi delle proteine sulla superficie della silice?
Mentre, come abbiamo già esposto (post
n.26), in ambiente acquoso la reazione di formazione dei polipeptidi è
impossibile, all’interno dei doppi strati elettrici si crea un microambiente
non acquoso che favorisce la formazione dei polipeptidi. Inoltre all’interno di
questi compartimenti entra in gioco una termodinamica a piccole scale, dove la
formazione del polipeptide diventa un processo spontaneo.
Quindi gli amminoacidi Levo accumulati
all'interno dei doppi strati elettrici della silice colloidale, all'interno di micro-cavità argillose, danno origine a
catene polipeptidiche avvolte intorno alla silice colloidale.
Le particelle di
silice colloidale hanno, però, un vita molto breve. Se una particella di silice
colloidale, sulla cui superficie si è sintetizzato un polipeptide, incontra
altre particelle di silice colloidale, si formerà silice amorfa. Le interazioni
elettriche tra particelle di silice colloidale sono così forti da deformarsi
reciprocamente.
Il polipeptide, non
trovando più le interazioni elettriche originarie, si stacca dalla superficie e
va in soluzione all'interno della cavità.
Poiché la
silice colloidale era elicoidale necessariamente elicoidale sarà anche
l’andamento dei polipeptidi. Queste strutture in soluzione sono
termodinamicamente instabili e, per effetto dell’agitazione termica e degli
urti con le molecole di acqua dovrebbero decomporsi in amminoacidi e cadere
nello stato 2 di energia.
Ma come abbiamo visto
nel post n. 18, la decomposizione dei polipeptidi in amminoacidi pur essendo
termodinamicamente possibile è cineticamente impossibile. Le molecole di acqua
non hanno, a temperatura ambiente l’energia sufficiente per spezzare tutti i legami
del polipeptide. La decomposizione avviene ma a velocità molto bassa; una
barriera energetica impedisce, quindi, una rapida decomposizione. I polipeptidi
contengono però, al suo interno, cariche positive e cariche negative.
Ciascun polipeptide, prima di essere decomposto lentamente dall’acqua in singoli amminoacidi e precipitare nello Stato 2 come previsto dalla termodinamica, stabilisce spontaneamente legami tra le cariche positive e negative che stabilizzano la struttura elicoidale. La formazione della struttura stabile e ordinata, denominata α-elica, libera energia che aumenta l’entropia universale. L’α-elica si trova quindi in una fossa energetica, Stato 1.
Ciascun polipeptide, prima di essere decomposto lentamente dall’acqua in singoli amminoacidi e precipitare nello Stato 2 come previsto dalla termodinamica, stabilisce spontaneamente legami tra le cariche positive e negative che stabilizzano la struttura elicoidale. La formazione della struttura stabile e ordinata, denominata α-elica, libera energia che aumenta l’entropia universale. L’α-elica si trova quindi in una fossa energetica, Stato 1.
È probabile però che
la composizione in amminoacidi delle α-eliche fosse diversa nelle diverse zone
del pianeta. Come gli esperimenti alla Miller hanno dimostrato, alcuni
amminoacidi si formano in condizioni particolari. Per esempio Metionina e
Cisteina si formano solo se nella miscela dell’atmosfere primordiale fosse
stato presente Idrogeno Solforato (H2S). Ma questo composto poteva
essere presente solo in vicinanza dei vulcani. Altri amminoacidi hanno bisogno
di alte temperature non raggiungibile con gli esperimenti di Miller (post n.
25). Dobbiamo quindi prendere in considerazione il fatto che probabilmente la
composizione delle α-eliche, sulla superfice del pianeta, poteva variare in
conseguenza di condizioni chimico-fisiche locali.
E allora, non si può non concludere che i polipeptidi, prodotti
dalle ordinarie forze chimico-fisiche e da condizioni chimico-fisiche locali,
sotto forma di α-elica, dovevano trovarsi, in epoca prebiotica, in grande
abbondanza, su tutta la superficie del pianeta, in ogni cavità, in ogni poro,
in ogni nicchia di masse argillose.
Ma come evidenzia Duranti Marcello in “Introduzione allo studio delle
proteine” 2015: «Alcune α-eliche contengono porzioni del cilindro idrofobiche,
ciò dà origine a interazioni tra amminoacidi idrofobici dando origine a
strutture super secondarie che sono il primo passo verso le strutture terziarie
delle proteine».
È probabile
quindi che all'interno di masse argillose, da alcune α-eliche, si siano formati spontaneamente
strutture super secondarie e successivamente, con ulteriori
aggregazioni, strutture terziarie o globulari, cioè enzimi ad ampio spettro di azione. La formazione delle strutture globulari, provoca l’espulsione di molecole di acqua che aumenta il caos universale e quindi termodinamicamente più stabili. La struttura terziaria occuperà adesso lo Stato 1, con un’energia inferiore di quella di due o tre singole α-eliche e sarà quindi termodinamicamente più stabile.
aggregazioni, strutture terziarie o globulari, cioè enzimi ad ampio spettro di azione. La formazione delle strutture globulari, provoca l’espulsione di molecole di acqua che aumenta il caos universale e quindi termodinamicamente più stabili. La struttura terziaria occuperà adesso lo Stato 1, con un’energia inferiore di quella di due o tre singole α-eliche e sarà quindi termodinamicamente più stabile.
Quanto esposto
fino adesso, cioè l’origine dei polipeptidi, è corredato in linea di massima da
dati sperimentali. Il cammino seguito dai
polipeptidi verso l’origine del proto organismo, e quindi verso l’origine della
vita, è per la scienza un vero mistero. Ora, impegnarsi nella ricerca di un
tale cammino si rischia, come scrisse Schrödinger, di rimediare una brutta
figura. Ma siccome non sono un accademico, io non rischio nessuna figuraccia e
quindi ci provo.
Non avendo a
disposizione dati sperimentali, per comprendere l’origine del proto-organismo,
possiamo procedere, con uno sforzo di logica e di immaginazione, solo attraverso
una narrazione credibile.
E allora, immaginiamo
una nicchia, una micro cavità all’interno di una massa argillosa dove si sono
accumulati qualche centinaio di α-eliche. Alcune α-eliche hanno dato origine a
strutture super secondarie e successivamente a strutture terziarie. Le
strutture terziarie o globulari contengono al loro interno gruppi idrofobi e
alla loro superficie gruppi idrofili con cariche elettriche residue. Strutture
terziarie e α-eliche erano, quindi, sicuramente circondate da cluster di acqua
a formare un complesso sistema interattivo proteico.
Volendo fare una
estrema sintesi, se immaginiamo che sulla superficie di un polipeptide si
trovano i residui con cariche negative, essi saranno avvolti da una nuvola di
molecole di acqua con Hδ+ orientato verso il negativo.
Nella zona di
contatto tra i due aggregati di acqua, l’acqua stessa si disporrà in modo da
minimizzare la repulsione elettrostatica.
Dentro la cavità,
tutti i componenti del sistema interattivo dovevano, quindi, essere compresi
all'interno di una macrostruttura ordinata, “quasi cristallina”, di acqua ed il
sistema interattivo proteico assumeva l’aspetto di un gel. A questa macrostruttura
possiamo estendere il concetto espresso da Peter W. Atkins in riferimento all’α-elica riportato nel Post n. 18: La disposizione
ordinata di tutte
le molecole di questa macrostruttura a gel è favorita rispetto ad un ammasso
irregolare in quanto corrisponde alla situazione di maggior caos dell’universo.
La macrostruttura è certamente dotata di un caos minore a causa della
disposizione ordinata, ma il caos universale è maggiore a causa dell’energia
che si libera al momento della formazione dei forti legami idrogeno.
Come il sasso sulla collina che ad ogni temporale
sprofonda sempre di più e diventa più stabile, cosi la macrostruttura è
precipitata in una fossa energetica, rappresentata dallo Stato 1, e presenta
una grande stabilità chimica.Questo sistema
interattivo tra molecole proteiche opera, quindi, all’interno
del secondo principio della termodinamica, dove è l’ordine a generare caos, la
formazione di strutture complesse a produrre entropia.All’interno di
questa struttura a gel i componenti del sistema comunicavano attraverso la
forza elettromagnetica generata dai potenziali di superficie. Ora è evidente
che se dall’ambiente esterno una o più molecole ricche di energia vengono a
contatto con il gel della micro cavità, il polipeptide che si trova in
prossimità inizia a destabilizzarsi cambiando forma. Tale cambiamento induce
l’acqua che avvolge il polipeptide ad assumere un’altra disposizione. Tale
nuova disposizione costringerà tutte le molecole di acqua del gel a
riorientarsi elettricamente passando l’informazione a tutte le macromolecole
del sistema che in misura grande o piccola saranno soggette a cambiamenti della
loro forma. L’energia accumulata da un singolo polipeptide, viene scaricata e
condivisa da tutto il complesso sistema interattivo. La nuova disposizione di
tutte le altre macromolecole del gel manderà un retrosegnale che indicherà alla
prima macromolecola se respingere o cooptare, se sintetizzare e cosa
sintetizzare. Avranno successo solo i sistemi che riusciranno ad elaborare un
sistema di comunicazione che minimizza gli errori. Il complesso sistema interattivo
è diventato un’entità e presenta una rudimentale omeostasi, cioè la capacità di
mantenere un equilibrio chimico uniforme più o meno costante in un ambiente
mutevole. L'omeostasi definita così è però solo un'idea, un concetto.
Ma come possiamo
rappresentarci fisicamente questa entità, e che cosa è veramente l’omeostasi?
La formazione
delle molecole dagli atomi coinvolge sempre cariche elettriche. Intorno alla
molecola di un composto dobbiamo immaginarci un campo elettromagnetico con un suo
contenuto energetico specifico, diverso di qualsiasi altro composto. Tale campo elettromagnetico conferisce le
proprietà al composto. Per esempio, in una goccia o in un bicchiere d’acqua il
campo elettromagnetico che avvolge tutte le molecole conferisce, a temperatura
ambiente, la liquidità dell’acqua. Il campo elettromagnetico che avvolge le
molecole di un amminoacido gli conferisce la solubilità in acqua. Quando decine
di amminoacidi si legano a formare una proteina enzimatica il campo elettromagnetico
intorno alla sua molecola non solo conferisce le proprietà intrinseche come la
solubilità, ma conferisce anche una funzione: la funzione enzimatica, cioè l’enzima,
attraverso il suo campo elettromagnetico, riconosce e scinde o lega molecole
specifiche. Quando centinaia di enzimi, avvolti da cluster di acqua, danno
origine ad un sistema interattivo proteico, precipitato in una fossa energetica
e quindi molto stabile, il campo elettromagnetico intorno e interno a tale
sistema, organizza e controlla il sistema stesso e lo identifica come entità. Ora, il campo
elettromagnetico dell’entità proteica genera sicuramente proprietà e funzioni, che a livello macroscopico si esplicano come omeostasi. Ma se l'entità è sotto il controllo del suo campo elettromagnetico, possiamo definire l'omeostasi come: la risposta del campo
elettromagnetico dell’entità rispetto a cambiamenti dell’ambiente esterno e del
mezzo interno. L’omeostasi è un’emergenza associata ad un complesso sistema
interattivo precipitato in una fossa energetica e quindi in equilibrio chimico.
L’omeostasi, attraverso reazioni chimiche e cicli di retroazione, tende a
preservare questo equilibrio. Poiché questa entità presenta omeostasi possiamo
identificarla come un primitivo
citoplasma proteico.
Emergenza la si
deve intendere sempre nel significato dato da Ernst Mayr (opera citata): «La
comparsa di caratteristiche impreviste in sistemi complessi». «Essa non racchiude
nessuna implicazione di tipo metafisica». «Spesso nei sistemi complessi
compaiono proprietà che non sono evidenti (né si possono prevedere) neppure
conoscendo le singole componenti di questi sistemi».
In realtà questo
è vero anche per i sistemi semplici. L’acqua è costituita da Idrogeno e
Ossigeno. Conoscendo le proprietà di questi due gas nessuno può prevedere le
proprietà dell’acqua. E questo è vero per tutti i composti chimici. Solo che
alle proprietà dei sistemi semplici e alle loro trasformazioni la chimica è
riuscita ad associare delle leggi. Per contro ai sistemi complessi che conducono
alla vita,che non presentano proprietà specifiche, noi associamo dei concetti.
L'omeostasi definita come la risposta del campo elettromagnetico dell'entità rispetto ai cambiamenti dell'ambiente esterno e del mezzo interno non è più un concetto, ma assume un significato chimico-fisico.
Il secondo
passaggio fondamentale verso l’origine del proto-organismo è la formazione di
corte molecole di RNA.
Ma come è
avvenuta la formazione dell’RNA?
L’RNA e
costituito da nucleotidi (post n. 31), questi ultimi sono formati dal legame
tra un gruppo fosfato (H2PO4-) e un nucleoside.
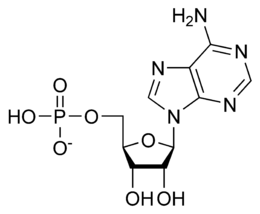
I costituenti dei
nucleosidi sono: uno zucchero, il D-Ribosio, appartenente alla famiglia degli
zuccheri (in basso nella figura), e una delle quattro basi azotate: Adenina
(nella figura) e Guanina, appartenenti alla famiglia delle Purine; Uracile e Citosina appartenenti
alla famiglia delle Pirimidine.
Si pone allora il
problema di capire se questi costituenti erano presenti in epoca prebiotica.
In relazione alle
basi azotate, nel 1961 Juan Orò uno dei chimici più impegnati in ricerche di
chimica prebiotica, riuscì a sintetizzare l’Adenina scaldando a 70°C una
elevata concentrazione di (HCN) acido cianidrico in presenza di ammoniaca (NH3).
In questo esperimento si ottennero parecchie sostanze organiche e tra queste
adenina. In seguito, Orò riuscì a sintetizzare anche la guanina. In merito a
questi esperimenti C. Ponnamperuma in “Origine della vita”, 1984 commenta: «[…] le concentrazioni usate da Orò
erano di gran lunga troppo alte per corrispondere a una situazione prebiotica.
Se le condizioni sperimentali fossero state davvero simili a quelle
prebiotiche, se, per esempio, si fossero usate concentrazioni più basse, allora
queste reazioni sarebbero di grande aiuto alla comprensione dell'origine delle
purine nelle condizioni presenti nella fase prebiotica della Terra».
Purtroppo dopo
questi esperimenti e per oltre 50 anni non risultano esperimenti significativi.
Come esposto nel
post n.7, il motivo è probabilmente da ricercare nella supponenza dei
sostenitori del “Mondo a RNA” che hanno trasformato un’ipotesi in un modello
confermato, considerando superflua la ricerca sui costituenti degli acidi
nucleici.
Dopo questo lungo
periodo sembrava che la ricerca sull’origine dei costituenti degli acidi
nucleici fosse caduta nell’oblio, quando due scienziati italiani Ernesto Di
Mauro e Raffaele Saladino riaprono la partita.
I loro
esperimenti descritti nel saggio “Dal big bang alla cellula madre l‘origine
della vita” 2016, sono di notevole interesse. Innanzitutto perché, invece di
utilizzare HCN (Acido cianidrico) che è un gas, hanno ottenuto le basi azotate
utilizzando la HCONH2 (Formammide) che ha un punto di ebollizione
oltre i 200°C, e che era sicuramente presente in epoca prebiotica perché
prodotta dalla reazione tra HCN e H2O. Inoltre tali esperimenti
avvengono utilizzando argilla o minerali sicuramente presenti in epoca
prebiotica. Questi esperimenti rientrano a pieno titolo nella teoria di Bernal.
Egli, infatti, aveva ipotizzato che l’argilla avrebbe potuto funzionare da
principio regolatore per selezionare, accumulare, proteggere e catalizzare le
sostanze fondamentali per l’origine della vita. Ci troviamo così ad avere, in
epoca prebiotica, le basi necessarie per l’acido nucleico proprio all’interno
di masse argillose, dove ha origine il primitivo citoplasma proteico.
In relazione al
Ribosio è da evidenziare che la sua molecola, come le molecole degli amminoacidi, presenta una forma Destro
e Levo, una l’immagine speculare dell’altra, ma solo il Destro viene utilizzato
negli acidi nucleici. Il Ribosio, come l’Arabinosio, lo Xilosio e il Lisosio, è
un pentamero della formaldeide (HCHO), nel senso che risulta formato da 5
molecole di formaldeide ma è, in soluzione acquosa, un composto instabile. Intorno
al 1880 A. Butlerov trattando la formaldeide in ambiente fortemente basico,
riuscì a sintetizzare il Ribosio, reazione nota come reazione del formoso. Questa
reazione non opera in condizioni prebiotiche, inoltre assieme al Ribosio si
sono forma una miscela di altri zuccheri, compresi gli altri tre pentameri, che
avrebbero intralciato la formazione dell’acido nucleico (post n.10). In
mancanza di ricerche valide, nel 1994 L. Orgel in Le scienze, “L’origine della vita sulla terra” scriveva:
«Innanzitutto, in mancanza di enzimi, è problematico sintetizzare ribosio in
quantità adeguate e con un sufficiente grado di purezza».
Nel 2008 in “Alle origini della vita” Christian
De Duve prende in considerazione le ricerche di Prieur (2001) e di Ricardo
(2004) i quali, utilizzando i borati sono riusciti a stabilizzare il Ribosio e
limitare a formazione di altri zuccheri. Ricardo, in “Planetary Organic Chemistry and the Origins of Biomolecules” 2015, descrive
nel dettaglio il meccanismo delle razioni e la funzione del boro ma riporta
anche le critiche di Hazen che definisce il boro un elemento “esotico” per la
chimica prebiotica. Christian De Duve riporta anche un lavoro di Ricardo et al.
2004 i quali hanno ottenuto i quattro pentosi (sia Destro che Levo) facendo
reagire gliceraldeide con glicolaldeide. Anche Di Mauro e Saladino richiamano i
lavori di Pieur e Ricardo ma aggiungono che simili risultati furono ottenuti
anche impiegando Zirconati. Ora, il fatto è che i zirconati sono tutt’altro che
“esotici”, essi, anche se in piccole quantità, si trovano distribuiti su tutta
la superfice del pianeta e principalmente in rocce sedimentarie e metamorfiche.
L’argilla, in relazione alla composizione, si distingue in caolinite,
beidellite e montmorillonite. Nell’argilla beidellite è stata trovata una
quantità di zirconati superiore alla media del pianeta. E così ci ritroviamo
ancora una volta all’interno della teoria di Bernal. Quindi, in epoca
prebiotica, oltre ad un primitivo citoplasma proteico contenute nelle cavità
dell’argilla, è probabile che decine di basi azotate e decine di zuccheri, sia
Destro che Levo, si trovassero diffuse all’interno di masse argillose. Da
questa miscela di basi azotate e zuccheri, diffuse nelle masse argillose,
soltanto quattro basi, Adenina, Citosina, Guanina e Uracile e solo un zucchero
il D-Ribosio sono stati cooptati all’interno del rudimentale citoplasma
proteico.
Ma perché
proprio questi e non gli altri, quale costrizione ha imposto tale selezione.
A selezionare
questi composti deve essere stata l’omeostasi del primitivo citoplasma
proteico.
L’omeostasi deputata
a mantenere l’equilibrio chimico permette, all'interno del citoplasma proteico,
solo la diffusione di sostanze che mantengono tale equilibrio.
Come abbiamo detto l'omeostasi, è la risposta del campo elettromagnetico dell'entità rispetto ai cambiamenti dell'ambiente esterno e del mezzo interno. E allora, proviamo a dare una rappresentazione fisica dell'omeostasi.
Come abbiamo detto l'omeostasi, è la risposta del campo elettromagnetico dell'entità rispetto ai cambiamenti dell'ambiente esterno e del mezzo interno. E allora, proviamo a dare una rappresentazione fisica dell'omeostasi.
Immaginiamo di
avere un bicchiere di acqua e di aggiungere zucchero. Possiamo
semplicisticamente dire che il campo elettromagnetico intorno alle molecole di
zucchero è compatibile con quello delle molecole di acqua e quindi lo zucchero
si scioglie in acqua. Se invece nel bicchiere mettiamo una goccia di olio, il
campo elettromagnetico intorno alla molecole dell’olio non è compatibile con
quello dell’acqua, l’olio non si miscela con l’acqua e si raccoglie alla sua superficie.
Ora, immaginiamoci come poteva essere il campo elettromagnetico generato,
intorno alla nostra entità proteica, da centinaia di α-eliche. Queste α-eliche erano costituite da L-amminoacidi ed avevano
tutte un andamento destrorso. Il campo elettromagnetico intorno all’entità
proteica doveva riflettere l’andamento elicoidale destrorso delle α-eliche e
quindi doveva essere necessariamente destrorso. Se l’entità proteica fosse stata
costituita da α-eliche sinistrorse, il campo elettrico sarebbe stato sinistrorso
cioè l’immagine speculare del campo elettrico dell’entità destrorsa. Ora, poiché
le molecole di D-Ribosio e di L-Ribosio sono una l’immagine dell’altra, anche il
loro campo elettrico deve essere uno l’immagine speculare dell’altro, cioè
destrorso e sinistrorso. E allora, quando in epoca prebiotica molecole di
D-Ribosio e di L-Ribosio cercarono di diffondere all’interno della cavità dove
si trovava un’entità di α-eliche destrorse, l'omeostasi ha cooptato il D-Ribosio destrorso perché complementare al campo elettrico dell’entità mentre la sua
immagine speculare, L-Ribosio sinistrorso, venne respinto.
Oltre al Ribosio nelle masse argillose
erano presente sicuramente altri zuccheri simili al Ribosio, anch’essi Destro e
Levo, come per esempio l’Arabinosio. Il D-Arabinosio al pari del D-Ribosio era
sicuramente complementare al campo elettrico dell’entità proteica. Ma perché è
stato scelto il D-Ribosio e non il D-Arabinosio.
Come si vede
dall’immagine la molecola di D-Arabinosio ha, rispetto al D-Ribosio un solo un
gruppo –OH a sinistra invece che a destra. Per questa piccola differenza
l’Arabinosio ha un punto di fusione di 157°C mentre il Ribosio ha un punto di
fusione di 90°C. Ma i punti di fusione sono determinati dalla interazione delle
cariche elettriche delle molecole, cioè in definitiva del campo
elettromagnetico intorno alle molecole. Quindi i campi elettromagnetici delle
molecole di D-Ribosio e di D-Arabinosio sono diversi. Ma come abbiamo già detto,
al campo elettromagnetico specifico di ogni molecola di qualsiasi composto è
associato un contenuto energetico specifico. Le molecole di D-Ribosio e
D-Arabinosio hanno perciò contenuti energetici diversi. Allora, se il campo
elettromagnetico intorno all'entità proteica ha scelto il D-Ribosio vuol dire
che il contenuto energetico delle sue molecole mantengono l’equilibrio
dell’entità proteica, mentre le molecole di D-Arabinosio lo avrebbero destabilizzato. L'omeostasi dell’entità
proteica riconosce quindi differenze di campo elettromagnetico e di livello
energetico delle molecole. Questo principio deve aver funzionato anche nella
scelta delle basi azotate. Solo i campi elettromagnetici associati alle
molecole di Adenina, Citosina, Guanina, Uracile sono compatibili con il campo
elettromagnetico intorno e interno all'entità proteica, e i loro livelli
energetici stabilizzano l’equilibrio termodinamico. In definitiva, l’omeostasi coopta le molecole dell’ambiente in base alla compatibilità
del campo elettromagnetico e al contenuto energetico.
Semplicisticamente
possiamo concludere che Adenina, Citosina, Guanina, Uracile e D-Ribosio solo
solubili nell'entità proteica mentre non lo sono tutte le altre basi azotate e
zuccheri.
L’entità proteica
che presenta omeostasi l’abbiamo identificato come primitivo citoplasma proteico.
Ma il rudimentale
citoplasma proteico altro non è che un insieme di enzimi. All’interno
dell’entità, questi enzimi utilizzando il poco fosfato a disposizione nella
soluzione, legano nel modo giusto il D-Ribosio con una delle basi e con fosfato
dando origine ai nucleotidi. Atri enzimi legano nel modo giusto tre nucleotidi
dando origine ai trinucleotidi. Come abbiamo ipotizzato nel post n. 27, in
epoca prebiotica doveva esistere una interazione diretta tra un trinucleotide e
un amminoacido specifico, un sistema chimico-fisico di riconoscimento e
complementarietà. Ora, quando i trinucleotidi diffondono all’interno
dell’entità e incontrano un’α-elica ogni trinucleotide si sovrappone
allo specifico amminoacido dell’α-elica.
Nel momento in cui ciascun amminoacido dell’α-elica è sovrapposto
dallo specifico trinucleotide sarà l’azione enzimatica dell’α-elica a legare i
trinucleotidi dando origine all’RNA, l’acido ribonucleico. Poiché l’RNA è stato sintetizzato da un enzima
elicoidale, l’α-elica, esso risulta avere una struttura
elicoidale. Se nella cavità erano
presenti un centinaio di α-eliche diverse, esse daranno origine a un centinaio
di RNA diversi. Gli RNA si sostituiscono alla silice e con gli
amminoacidi in soluzione potranno sintetizzare gli enzimi che per varie cause
venivano decomposti. Per utilizzare
la metafora di Cairns-Smith: l’armatura, la silice, ha generato un arco, l’α-elica, che a sua volta ha generato
un’armatura, RNA, che si sostituisce definitivamente alla prima. La
sintesi dei nucleotidi (Ribosio + base azotata +gruppo fosfato), la sintesi dei
trinucleotidi e la sintesi dell’RNA avvengono tutte nel microambiente non acquoso
della superfice degli enzimi. Queste condizioni permettono all’enzima una
reattività straordinaria e diversa dalle reazioni in ambiente acquoso. Inoltre
in tutte queste reazioni di sintesi si liberano molecole di acqua che andranno ad
aumentare il caos universale. Si crea ancora ordine aumentando l’entropia: Caos
dall’ordine.
Con la comparsa degli RNA l’entità si
amplia dando origine ad un citoplasma contenente un sistema interattivo Acidi
nucleici-Enzimi che sprofonda ancora di più nella fossa energetica. L'omeostasi mantiene l'equilibrio chimico attraverso il campo elettromagnetico intorno e interno all'entità
La nuova entità,
cioè il citoplasma Acidi nucleici-enzimi, è il proto-organismo.
In conclusione, il
secondo principio della termodinamica non potendo seguire la via del massimo caos rappresentata
dalla fossa energetica dello stato 2, segue il cammino del caos possibile e
scava una fossa energetica parallela rappresentata dallo stato 1.
Lu Lungo questo cammino, attraverso salti successivi l’ordine genera caos fino a dare origine al proto-organismo. Si è sempre considerato il proto-organismo come un sistema lontano dall’equilibrio termodinamico descritto dallo stato 2. In realtà il proto-organismo è un sistema lontano dal caos massimo ma è in equilibrio con il caos possibile e quindi sotto il controllo del 2° principio della termodinamica.
Lu Lungo questo cammino, attraverso salti successivi l’ordine genera caos fino a dare origine al proto-organismo. Si è sempre considerato il proto-organismo come un sistema lontano dall’equilibrio termodinamico descritto dallo stato 2. In realtà il proto-organismo è un sistema lontano dal caos massimo ma è in equilibrio con il caos possibile e quindi sotto il controllo del 2° principio della termodinamica.
E allora, questo
è lo scenario che ci troviamo di fronte.
In miliardi e
miliardi di cavità, nicchie, anfratti e spazi inter-cristallini di un
imprecisato ma enorme numero di masse argillose si sintetizzano un numero
infinito di polipeptidi che danno origine ad un primitivo citoplasma proteico. Molecole
di basi azotate e di D-Ribosio contenute nelle masse argillose che vengono
cooptate all’interno del citoplasma proteico. Polipeptidi elicoidali che
sintetizzano l’acido nucleico. L’interazione acidi nucleici-enzimi dà origine
ad un numero sterminato di proto-organismi.
Giovanni
Occhipinti
Prossimo articolo: Dal proto-organismo alla cellula ( fine Marzo)