Post n. 11
NOI, GLI ALIENI LA MATERIA. Ma un'altra vita è possibile. Gli amminoacidi
Dunque,
gli elementi biogeni(C, N, O, H) sono gli unici che, attraverso i loro
composti, sono adatti a svolgere, negli organismi viventi, le numerose funzioni
biologiche. Sappiamo che tra questi composti i più importanti sono gli acidi
nucleici, DNA e RNA, e le proteine.
Le proteine costituiscono tessuti
e organi, permettono alle cellule di comunicare, controllano ciò che deve entrare
e uscire dalla cellula, fungono da anticorpi.
Tutti gli organismi viventi hanno
anche una complessità di funzioni interdipendenti che permette loro: la nutrizione,
la crescita, la riproduzione, l’evoluzione, la reazione agli stimoli, la morte.
Tutte queste funzioni vitali hanno in comune il metabolismo; cioè quel processo
di reazioni chimiche coadiuvate da proteine (enzimi)
che permettono agli organismi viventi di funzionare. All’interno della cellula
si trovano migliaia di enzimi che regolano e programmano migliaia di reazioni
chimiche, nessuna reazione biologica e nessuna delle funzioni sopra elencate
può avvenire senza il loro intervento, nemmeno la sintesi degli acidi nucleici.
Le proteine sono macromolecole i
cui costituenti sono gli amminoacidi.
Ma gli amminoacidi, in epoca
prebiotica, erano presenti sul nostro pianeta?
Nel 1953 S.L. Miller, ipotizzando un’atmosfera primordiale costituita
da CH4, NH3, H2O e H2,
riuscì, con apporti di energia elettrica, ad ottenere diverse sostanze
organiche e, tra queste, parecchi amminoacidi alcuni dei quali componenti delle
nostre proteine. Questo esperimento, condotto in condizioni prebiotiche
plausibili, segnò la data di nascita della chimica prebiotica.
Negli
anni che seguirono furono compiute diverse verifiche che confermarono i
risultati dell’esperimento di Miller. Inoltre diversi ricercatori hanno
eseguito esperimenti sia variando la composizione della miscela gassosa sia le
fonti di energia. Tutti questi lavori hanno confermato che in epoca prebiotica,
sul nostro pianeta, era possibile la sintesi di un grande numero di sostanze
organiche e tra queste spesso erano presenti amminoacidi. Attraverso questi
esperimenti è stata dimostrata la presenza, in epoca prebiotica, di circa 60
amminoacidi diversi. Inoltre è stata dimostrata anche la presenza di acido
cianidrico, (HCN), precursore delle purine, di aldeide formica, (HCHO),
precursore del ribosio e di altre importanti sostanze organiche tra cui l’urea.
È
rimarchevole il fatto che le stesse sostanze, in particolare gli amminoacidi,
siano stati trovati nei meteoriti risalenti all’epoca della formazione del
nostro sistema solare. La scoperta degli amminoacidi negli esperimenti di
Miller e la loro presenza nei meteoriti dimostra, secondo gli scienziati, la
facilità di sintesi di questi composti. Perfino i sostenitori del “Mondo a RNA” non hanno dubbi sulla presenza degli
amminoacidi in epoca prebiotica. Manfred Eigen, in riferimento agli esperimenti
alla Miller, in “Gradini verso la vita”, 1992 afferma: «Ciò che rende
significativi questi esperimenti è non tanto il fatto che si formino in
generale amminoacidi, ma che le loro frequenze relative corrispondano a quelle
che si riscontrano in natura, e in particolare nei composti organici scoperti
nei meteoriti. »
Agli
inizi degli anni ’90, alcuni ricercatori hanno messo in dubbio la presenza di
un’atmosfera primordiale costituita da CH4, NH3,
H2O e H2. Questi ricercatori hanno ipotizzato
un’atmosfera primordiale costituita da CO2, N2, e H2O,
e in tali condizioni la formazione degli amminoacidi con apporti di energia non
si verifica. Miller ha definito questi lavori ipotesi senza dati a sostegno.
Nessuna
ricerca seria ha mai messo in dubbio la presenza di amminoacidi in epoca
prebiotica.
Possiamo
concludere che numerosi e forti indizi dimostrano la presenza degli amminoacidi
in epoca prebiotica. Dalla sintesi di queste molecole hanno origine le proteine.
Ma
perché gli amminoacidi? E poi, sono possibili altre soluzioni?
Secondo
le mie limitate conoscenze, in sessant’anni di chimica prebiotica, l’unico
scienziato che ha cercato di dare una risposta a queste domande è stato Mario
Ageno in “Lezioni di Biofisica 3” 1984.
Il
Prof. Mario Ageno parte dalla constatazione che le cellule degli organismi
viventi non contengono molecole di dimensioni intermedie, ma sono costituite
da:
a)
piccole molecole, il più possibili semplici, che si trovino già nell’ambiente o
facili da sintetizzare
b)
polimeri lineari (macromolecole) realizzati con operazioni ripetitive di un
numero limitato di piccole molecole (monomeri).
Come
noto i polimeri lineari, si possono ottenere sia per poliaddizione
che per policondensazione. La poliaddizione si
ottiene dall’unione
 |
| it.wikipedia.org/wiki/Polietilene |
di migliaia ma anche di milioni di molecole dello stesso
tipo. Essa è la ripetizione dello stesso motivo senza nessun contenuto di
informazione, porta a polimeri generalmente di tipo lineari, per esempio il
polietilene, ed avviene attraverso un processo chimico abbastanza complesso.
La
policondensazione può avvenire anche tra molecole diverse, attraverso
l’eliminazione di molecole di acqua. Questo tipo di polimerizzazione non può
avvenire in presenza di acqua, tuttavia il processo chimico è molto più
semplice della poliaddizione. Essa può condurre a materie plastiche, ma viene
utilizzata dagli organismi viventi per la costruzione delle macromolecole
necessarie alla vita. Infatti, non essendo la ripetizione monotona di uno
stesso motivo, i polimeri risultanti possono contenere una elevata
informazione.
Secondo
Ageno la scelta dei polimeri lineari ha una sua logica costruttiva estremante
semplice, partendo da un numero limitato di pezzi, sempre con la stessa
operazione costruttiva, si realizzano strutture molecolari diverse ma tutte
imparentate tra di loro. Probabilmente esistono altre soluzioni per
immagazzinare informazioni e funzioni ma tutte sono molto più complicate. La
soluzione più conveniente da un punto di vista evolutivo sembra essere proprio
quella dei polimeri lineare. In definitiva l’evoluzione ha scelto il processo
polimerico più semplice, la policondensazione, e i polimeri più semplici cioè i
polimeri lineari e Ageno aggiunge: «Sembra dunque molto probabile che, dovunque
appaiono sotto la spinta di cause naturali sistemi in qualche modo simili per
le loro caratteristiche generali agli organismi viventi che noi conosciamo,
questi sistemi si basino per la loro riproduzione su una qualche specie di
polimero lineare. Se non altro, questa soluzione si raggiunge più facilmente e
prima di ogni altra nel corso di una evoluzione chimica che prenda le mosse (il
che è inevitabile) da piccole molecole costituite da pochissimi atomi. E
allora, quali monomeri una volta accettata la soluzione del polimero lineare?»
Egli
esaminando i costituenti delle proteine si pone la domanda: «Che cosa si può
immaginare di più semplice
 |
| it.wikipedia.org/wiki/Amminoacido |
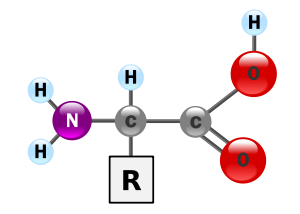
di un amminoacido, come elemento strutturale di un
polimero lineare?» Si tratta in sostanza di un atomo di carbonio che stabilisce
un legame con il più semplice degli elementi, l’H. Un secondo legame avviene
con la più semplice delle funzioni basiche, -NH2. Un terzo legame
avviene con la più semplice funzione acida –COOH. Per ultimo il quarto legame
avviene con un residuo (R) generalmente di un idrocarburo semplice o di un suo
derivato. Egli conclude, che la facilità con cui essi si trovano in natura per
esempio nei meteoriti, dimostra che si tratta di molecole semplici e facili da
sintetizzare e suggeriscono la conclusione che le catene polipeptidiche
rappresentano la soluzione più semplice.
Quindi,
alla domanda: perché gli amminoacidi? La risposta è: perché sono semplici e
facili da sintetizzare.
Ora,
la questione è che essi sono sì semplici e facili da sintetizzare ma presentano
una complessità di proprietà senza le quali la vita non potrebbe esistere. Tale
complessità ci pone, come vedremo, una spinosa domanda sul problema
dell’origine della vita che normalmente non cade nell’ambito della scienze
fisiche.
Quando
Ageno parla di polimeri lineari, si riferisce alla struttura primaria cioè alla
disposizione e alla struttura degli amminoacidi nella catena polimerica.
Il
fatto è che se la struttura primaria rimasse tale, cioè semplicemente un lungo
polimero, essa non esplicherebbe nessuna funzione vitale. In realtà le singole
proteine oltre alla struttura primaria, presentano una struttura secondaria e
una struttura terziaria. Le proteine svolgono le loro funzioni vitali solo
ricorrendo alle strutture secondarie e terziarie.
Per
comprendere come sono possibile tali nuove strutture è necessario esaminare le
proprietà degli amminoacidi.
1)
La prima caratteristica degli amminoacidi è proprio quella di essere molecole
semplici e facili da sintetizzare in ambiente prebiotico.
2)
Una seconda proprietà è che gli amminoacidi sono solubili in acqua e stabili.
Se non fossero solubili in acqua la vita non esisterebbe, poiché essi si
sarebbero raccolti insieme come grumi di catrame o come chiazze oleose alla
superfice dei bacini idrici.
3)
Gli esperimenti di Miller hanno evidenziato la presenza, in epoca prebiotica,
di circa 60 amminoacidi diversi, ma la vita ne utilizza solo 20. Se essi avessero
potuto reagire in acqua avrebbero dato origine ad un numero enorme di
polipeptidi, di composizione e lunghezze casuali, ma di nessun interesse per
l’origine della vita. Quindi gli amminoacidi devono essere sì solubili in acqua
ma non devono reagire in acqua. E infatti essi realizzano polimeri attraverso
la policondensazione che in acqua
 |
| biochimica.bio.uniroma1.it |
non è permessa.
4)
Il legame peptidico è un legame che si realizza tra
il gruppo –COOH di un amminoacido e il gruppo –NH2 di un altro
amminoacido con eliminazione di una molecola di H2O.
La
caratteristica di questo legame è di essere un legame in risonanza. Cioè il doppio
legame tra l’atomo di carbonio e l’
ossigeno non è localizzato tra i due
atomi ma
 |
| www.unitus.it |
è distribuito anche sul legame C-N. La conseguenza di questa
delocalizzazione è che ogni zona del legame peptidico della proteina giace su
un piano e la molecola della proteina non può ruotare attorno ai legami
peptidici. Come abbiamo detto, le proteine non sono soltanto lunghe catene
lineari di amminoacidi. Questa è solo ciò che viene chiamata struttura
primaria. Le singole proteine presentano una struttura secondaria e una
struttura terziaria attraverso le quali esse svolgono le loro funzioni vitali.
Nelle struttura secondaria esse realizzano strutture a elica e a fogli, dette
α-eliche e fogli-β. Ebbene,
 |
| orig. da: it.foldit.wikia.com |
5)
Una seconda condizione affinché queste strutture secondarie possano realizzarsi
è che le molecole costituenti siano asimmetriche. Sappiamo che gli amminoacidi,
tranne la glicina, sono chirali cioè esistono in
due forme asimmetriche una l’immagine speculare dell’altra denominate Destro e
Levo.
 |
| bios-project.blogspot.com |
Molecole simmetriche non possono realizzare né α-eliche né fogli-β. Le
strutture secondarie delle proteine si possono realizzare scegliendo una delle
due forme asimmetriche; negli organismi viventi è stata scelta la forma L.
6)
Un’altra caratteristica importante del legame peptidico è la presenza di un
atomo di idrogeno legato all’azoto. Il legame tra questi due elementi è un legame polarizzato che dà origine ad -Hδ+. Come
si vede dall’immagine dell’α-elica (tratteggio), esso si lega al -COδ-
di un altro amminoacido e sono questi legami che stabilizzano l’α-elica. Senza
questi legami la struttura secondaria α-elica delle proteine non potrebbe
esistere.
7)
Per finire, abbiamo visto che negli amminoacidi il carbonio è legato ad un
residuo R. Questi residui non sono scelti a caso. Alcuni di essi sono idrofili,
miscibili con l’acqua, altri sono idrofobi, non miscibili con l’acqua. Nella
struttura terziaria della proteina, cioè la struttura globulare,
gli R idrofobi si concentrano all’interno e gli R idrofili nella parte esterna.
Il risultato finale è che la proteina risulta molto stabile ed è difesa dalla
degradazione dell’acqua.
È
noto che i composti della chimica organica sono circa 1,5 milioni e raggruppati
in famiglie. Non esiste un’altra famiglia di composti organici che presenta
simili caratteristiche: gli amminoacidi sono unici, il passaggio fu obbligato.
Si
potrebbe concludere che gli amminoacidi sono composti versatili. Ma noi abbiamo
di fronte la vita e se vogliamo cercare di capire la sua origine alla domanda
iniziale: perché gli amminoacidi? Non basta più la risposta: sono semplici e
facili da sintetizzare; perché in realtà essi devono
possedere le seguenti caratteristiche:
1)
Semplici e facili da sintetizzare
2)
Solubili e stabili in acqua.
3)
Non devono reagire in acqua.
4)
Si devono legare tra di loro dando origine ad un legame peptidico in risonanza
5)
Devono essere chirali.
6)
Devono contenere un -Hδ+ residuo sull’atomo di azoto.
7)
Il residuo R non è casuale.
Se
fosse mancata solo una di queste proprietà, non sappiamo come sarebbe stata la
vita, o forse non esisterebbe. Gli amminoacidi sono composti unici.
Allora
la domanda è: ma come fanno a trovarsi negli amminoacidi tutte queste
proprietà, proprio lì in quei composti unici semplici e facili da sintetizzare,
giusto quelle proprietà necessarie alla vita, mentre la vita è ancora in
divenire?
Sette
colpi di fortuna?

Nessun commento:
Posta un commento